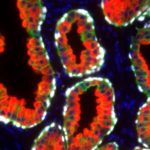
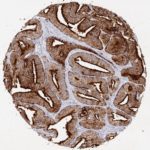
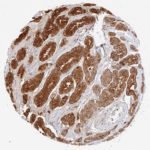
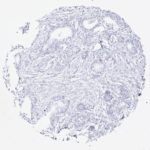
Der Anti-PSA (Prostata-spezifisches Antigen)-Klon HAM18 sticht unter mehr als 1.000 kommerziell erhältlichen PSA-Antikörpern wegen seiner nachgewiesenen hohen Spezifität und Empfindlichkeit für die Erkennung von Prostatakrebs hervor. Obwohl PSA ausschließlich in Prostata-Epithelzellen exprimiert wird, haben Studien mit verschiedenen anderen Antikörpern die PSA-Expression bei 9%-60% der Brustkrebse 1-8, bei 55% der malignen Melanome 7, 3%-9% der männlichen Brustkrebse 8, 9, 3 von 3 azinären Pankreaskarzinomen 10, verschiedenen Speicheldrüsenkarzinomen (einschließlich 6 von 11 pleomorphen Adenomen, 1 von 6 Mukoepidermoidkarzinomen und 1 von 2 nicht anderweitig spezifizierten Adenokarzinomen) 11-13 beschrieben. In multiplen Fallberichten wurde die PSA-Expression auch in mindestens 4 Fällen von paraurethralem Adenokarzinom 14-18 und in einem Harnblasenkarzinom 19 beschrieben. Darüber hinaus wurde beschrieben, dass die PSA-Expression in normalen Speicheldrüsen, 60% der Speicheldrüsenadenome und im normalen Pankreasepithel 12 vorkommt. Bei Verwendung des Anti-PSA-Klons HAM18 wurde in keinem dieser normalen und neoplastischen Gewebe eine PSA-Positivität festgestellt.
Die Validierung des Anti-PSA-Klons HAM18 bei mehr als 20.000 Krebsarten unter Verwendung des von Oncodianova empfohlenen Protokolls bei einer Antikörperverdünnung von 1:800 ermöglichte eine genaue Dokumentation der Sensitivität und Spezifität dieses Antikörpers. Die wichtigsten Kennzahlen zur Leistungsfähigkeit des Anti-PSA-Antikörpers HAM18 lauten wie folgt.
Sensitivität
| Prostate Cancer Subset | Samples analyzed (n) | PSA positive (n) | Sensitivity at 1:800 (1:100) dilution |
| Gleason 3+3=6 | 2,439 | 2,437 | 99.92% |
| Gleason 3+4=7 | 7,470 | 7,461 | 99.87% |
| Gleason 4+3=7 | 2,213 | 2,205 | 99.64% |
| Gleason 8 | 112 | 111 | 99.15% |
| Gleason 9-10: | 628 | 618 | 98.41% |
| Recurrent prostate cancer after therapy (Gleason ≥8) | 392 | 387 | 99.72% |
| Small cell carcinoma of the prostate | 13 | 1 | 7.69% |
Spezifikation
| Tumor type | Samples analyzed (n) | PSA positive (n) | Specificity at 1:800 dilution |
| Adenocarcinoma,
extraprostatic |
877 | 1* | 99.89% |
| Squamous cell carcinoma, extraprostatic | 319 | 0 | 100% |
| Small cell carcinoma,
extraprostatic |
46 | 0 | 100% |
| Other extraprostatic carcinomas | 1,603 | 0 | 100% |
| All extraprostatic
malignancies |
2,845 | 1 | 99.96% |
*Weak extraprostatic PSA positivity was seen in 1 of 30 endometroid ovarian cancers
Die Verwendung von hoch validierten Antikörpern wird für zertifizierte und akkreditierte Pathologielabors dringend empfohlen.
In der diagnostischen Routine kann die PSA (HAM18)-Immunhistochemie bei den folgenden Anwendungen eingesetzt werden:
- Karzinom unbekannter Herkunft: Nachweis oder Ausschluss der Herkunft von Prostatakrebs.
- Blasentumor bei männlichen Patienten ohne eindeutige urotheliale Vorläuferläsion, die auf einen urothelialen Ursprung schließen lässt: Herkunft von einem Prostatakarzinom ausschließen.
- Fortgeschrittener hochgradiger Prostatakrebs mit eher niedrigen (oder unbekannten) PSA-Werten im Serum: Eine niedrige PSA-Expression bei schlecht differenziertem Krebs deutet darauf hin, dass die Serum-PSA-Werte die gesamte Tumormasse des Patienten “unterschätzen” können.
Reference for clone HAM18:
Bonk S et al. Prognostic and diagnostic role of PSA immunohistochemistry: A tissue microarray study on 21,000 normal and cancerous tissues. Oncotarget 2019 (10): 5439-5453. https://doi.org/10.18632/oncotarget.27145
Further References
[1] Poh BH, Jayaram G, Sthaneshwar P, Yip CH: Prostate-specific antigen in breast disease. Malays J Pathol 2008, 30:43-51.
[2] Alanen KA, Kuopio T, Collan YU, Kronqvist P, Juntti L, Nevalainen TJ: Immunohistochemical labelling for prostate-specific antigen in breast carcinomas. Breast Cancer Res Treat 1999, 56:169-76.
[3] Heyl W, Wolff JM, Biesterfeld S, Schroder W, Zitzelsberger D, Jakse G, Rath W: Immunohistochemical analysis of prostate-specific antigen does not correlate to other prognostic factors in breast cancer. Anticancer Res 1999, 19:2563-5.
[4] Miller MK, Unger PD, Bleiweiss IJ: Immunohistochemical analysis of prostate specific antigen in breast cancer. Breast Cancer Res Treat 2001, 68:111-6.
[5] Ilvan S, Celik V, Cetinaslan I, Calay Z, Ferahman M: Immunohistochemical analysis of prostate-specific antigen in female breast cancer. J BUON 2004, 9:183-6.
[6] Narita D, Cimpean AM, Anghel A, Raica M: Prostate-specific antigen value as a marker in breast cancer. Neoplasma 2006, 53:161-7.
[7] Bodey B, Bodey B, Jr., Kaiser HE: Immunocytochemical detection of prostate specific antigen expression in human primary and metastatic melanomas. Anticancer Res 1997, 17:2343-6.
[8] Kraus TS, Cohen C, Siddiqui MT: Prostate-specific antigen and hormone receptor expression in male and female breast carcinoma. Diagn Pathol 2010, 5:63.
[9] Carder PJ, Speirs V, Ramsdale J, Lansdown MR: Expression of prostate specific antigen in male breast cancer. J Clin Pathol 2005, 58:69-71.
[10] Kuopio T, Ekfors TO, Nikkanen V, Nevalainen TJ: Acinar cell carcinoma of the pancreas. Report of three cases. APMIS 1995, 103:69-78.
[11] van Krieken JH: Prostate marker immunoreactivity in salivary gland neoplasms. A rare pitfall in immunohistochemistry. Am J Surg Pathol 1993, 17:410-4.
[12] Elgamal AA, Ectors NL, Sunardhi-Widyaputra S, Van Poppel HP, Van Damme BJ, Baert LV: Detection of prostate specific antigen in pancreas and salivary glands: a potential impact on prostate cancer overestimation. J Urol 1996, 156:464-8.
[13] James GK, Pudek M, Berean KW, Diamandis EP, Archibald BL: Salivary duct carcinoma secreting prostate-specific antigen. Am J Clin Pathol 1996, 106:242-7.
[14] Svanholm H, Andersen OP, Rohl H: Tumour of female paraurethral duct. Immunohistochemical similarity with prostatic carcinoma. Virchows Arch A Pathol Anat Histopathol 1987, 411:395-8.
[15] Spencer JR, Brodin AG, Ignatoff JM: Clear cell adenocarcinoma of the urethra: evidence for origin within paraurethral ducts. J Urol 1990, 143:122-5.
[16] Zaviacic M, Sidlo J, Borovsky M: Prostate specific antigen and prostate specific acid phosphatase in adenocarcinoma of Skene’s paraurethral glands and ducts. Virchows Arch A Pathol Anat Histopathol 1993, 423:503-5.
[17] Ebisuno S, Miyai M, Nagareda T: Clear cell adenocarcinoma of the female urethra showing positive staining with antibodies to prostate-specific antigen and prostatic acid phosphatase. Urology 1995, 45:682-5.
[18] Sloboda J, Zaviacic M, Jakubovsky J, Hammar E, Johnsen J: Metastasizing adenocarcinoma of the female prostate (Skene’s paraurethral glands). Histological and immunohistochemical prostate markers studies and first ultrastructural observation. Pathol Res Pract 1998, 194:129-36.
[19] Grignon DJ, Ro JY, Ayala AG, Johnson DE, Ordonez NG: Primary adenocarcinoma of the urinary bladder. A clinicopathologic analysis of 72 cases. Cancer 1991, 67:2165-72.