Spezifische Referenzen von der Jahrestagung der American Association of Cancer Research (AACR) 2020
Proceedings: AACR Annual Meeting 2020; April 27-28, 2020 and June 22-24, 2020; Philadelphia, PA, Volume 80, Issue 16 Supplement, pp. 3870 and pp. 4970
Abstract 3870:
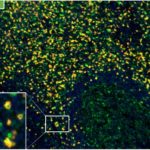
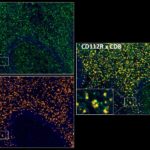
Patterns of CD112R expression in normal lymphatic tissues, inflammation and cancer
DOI https://doi.org/10.1158/1538-7445.AM2020-3870
Abstract 4970:
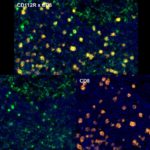
Prognostic role of CD112R, PD-1 and Ki67 expression in CD8+cytotoxic T cells in colorectal cancer
DOI https://doi.org/10.1158/1538-7445.AM2020-4970
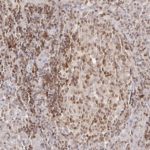
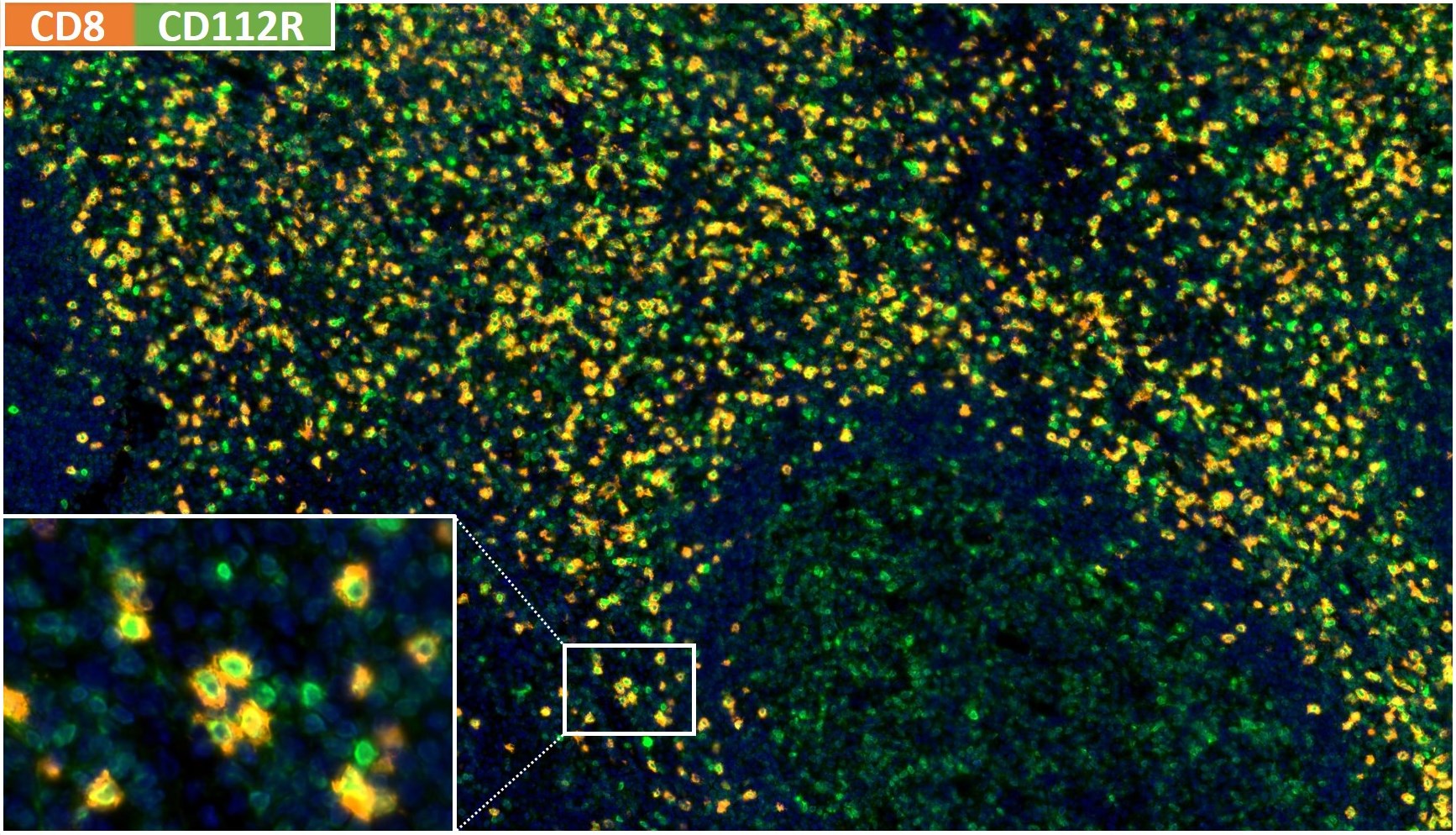
Der anti-PVRIG/CD112R Klon R12 wurde für den Nachweis von CD112R in Formalin-fixierten und in Paraffin eingebetteten Gewebeproben (IHC FFPE) entwickelt. Neben der Hellfeld-Mikroskopie zeigt der Antikörper seine Qualität insbesondere in der Mehrfarben-Immunfluoreszenz (Multiplex IHC). Die Sensitivität und Spezifität des anti-PVRIG/CD112R Klones R12 wurde an zahlreichen Normal- und Tumorgeweben intensiv validiert.
Der Antikörperklon R12 zeigt keinen Hintergrund in nicht-lymphoiden Zellen und in epithelialen Zellen. Aufgrund seiner hohen Spezifität in Kombination mit einem inhärent hohen Signal-zu-Hintergrund Verhältnis eignet sich R12 ideal für Multiplex-IHC Studien an humanen Geweben.
Die ersten klinischen Studien mit Inhibitoren der Immuncheckpoint-Marker CTLA4 und PD-1 zeigten bereits, dass die Blockade der Liganden-Rezeptor Bindung an diesem Checkpoint die Immunabwehr gegen Tumorzellen verstärkt. Ein weiterer Immuncheckpoint, nämlich die Achse TIGIT-PVR/PVRL2, ist zu einem vielversprechenden Ziel in der Tumor-Immuntheraphie geworden. TIGIT (T cell immunoglobulin and ITIM domain) und CD226 bilden einen Signalweg auf T-Zellen und fungieren jeweils als co-stimulatorische und co-inhibitorische Rezeptoren für die Liganden CD155 und CD112. Die TIGIT Signal-Achse insgesamt bildet ein komplexes Netzwerk mit weiteren Markern wie CD112R, CD96 and DNAM-1, die alle als mögliche Zielstrukturen für eine immunotherapeutische Intervention gesehen werden.
CD112R gehört zur Familie der Poliovirus-Rezeptor ähnlichen Proteine. CD112R wird insbesondere auf T-Zellen exprimiert und hemmt Signale, die durch den T-Zell Rezeptor vermittelt werden. CD112R bindet den Liganden CD112, der von vielen Antigen-präsentierenden Zellen und auch von Tumorzellen exprimiert wird. CD112R konkurriert mit CD226 um die Bindung an CD112 und fungiert dabei als co-inhibitorischer Rezeptor für T-Zellen. Eine Blockade der CD112R-CD112 Interaktion kann die T-Zell Antwort verstärken.
Die Mitglieder der Poliovirus Rezeptor (PVR)-Familie wurden ursprünglich als Mediatoren epithelialer Zell-Kontakte bekannt und zeigten zudem Funktionen bei der Signalvermittlung auf T-Zellen. Dabei interagieren die beiden Liganden, CD112 (PVRL2/Nectin-2) und CD155 (PVR/Necl-5) mit CD226 (DNAM-1), um T-Zellen zu stimulieren. Durch Bindung eines weiteren co-inhibitorischen Rezeptors, TIGIT (T cell Ig and immunoreceptor tyrosine-based inhibitory motif (ITIM) domain) wird die T-Zell Antwort unterdrückt. Die Bindung von TIGIT und CD112 ist sehr schwach. CD155 scheint der Hauptligand in diesem komplexen Netzwerk zu sein. CD96 (ein PVR-verwandtes Protein auf T-Zellen und NK-Zellen) bindet CD155, aber nicht CD112.
Die Erforschung der Beziehungen in diesem komplexen Netzwerk zwischen Liganden und Rezeptoren für CD112, wie CD112R, CD226 und TIGIT wird zu einem tieferen Verständnis für neue immuntherapheutischer Ansätze beitragen.
CD112R Antikörper Produktdetails
r